Αξιωματούχοι του FDA (Αμερικανικός Οργανισμός Τροφίμων και Φαρμάκων) προειδοποίησαν ότι το αντιβιοτικό κλαριθρομυκίνη (clarithromycin) μπορεί να αυξήσει τον κίνδυνο καρδιαγγειακών προβλημάτων ή θανάτου χρόνια αργότερα μετά τη λήψη του. Οι γιατροί θα πρέπει να δίνουν προσοχή όταν συνταγογραφούν το αντιβιοτικό και ιδιαίτερα σε ασθενείς με καθιερωμένη καρδιακή νόσο.
Η νέα σύσταση έγινε μετά από μια δεκαετή δοκιμή παρακολούθησης ασθενών με στεφανιαία νόσο οι οποίοι υποβλήθηκαν σε θεραπεία με το αντιβιοτικό.
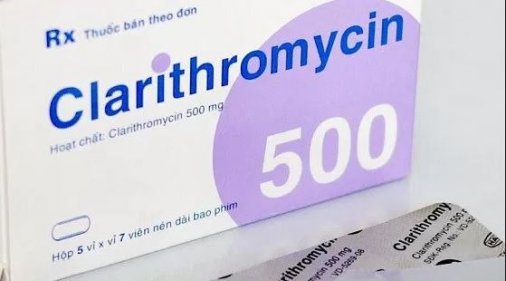 Η κλαριθρομυκίνη χρησιμοποιείται συνήθως για τη θεραπεία λοιμώξεων του δέρματος, του αυτιού, του κόλπου, του πνεύμονα και άλλων οργάνων του σώματος. Χρησιμοποιείται για τη θεραπεία της φαρυγγίτιδας, της αμυγδαλίτιδα και της οξείας ιγμορίτιδας, μεταξύ άλλων. Επιπλέον, μερικές φορές χρησιμοποιείται για τη θεραπεία της νόσου των λεγεωναρίων, την εκρίζωση του ελικοβακτηρίου του πυλωρού (Helicobacter pylori) και της νόσου Lyme. Οι αξιωματούχοι του FDA σημείωσαν ότι το αντιβιοτικό χρησιμοποιείται συνήθως για τη θεραπεία της μόλυνσης από το Mycobacterium avium που προκαλεί λοίμωξη των πνευμόνων και συχνά επηρεάζει τα άτομα με HIV.
Η κλαριθρομυκίνη χρησιμοποιείται συνήθως για τη θεραπεία λοιμώξεων του δέρματος, του αυτιού, του κόλπου, του πνεύμονα και άλλων οργάνων του σώματος. Χρησιμοποιείται για τη θεραπεία της φαρυγγίτιδας, της αμυγδαλίτιδα και της οξείας ιγμορίτιδας, μεταξύ άλλων. Επιπλέον, μερικές φορές χρησιμοποιείται για τη θεραπεία της νόσου των λεγεωναρίων, την εκρίζωση του ελικοβακτηρίου του πυλωρού (Helicobacter pylori) και της νόσου Lyme. Οι αξιωματούχοι του FDA σημείωσαν ότι το αντιβιοτικό χρησιμοποιείται συνήθως για τη θεραπεία της μόλυνσης από το Mycobacterium avium που προκαλεί λοίμωξη των πνευμόνων και συχνά επηρεάζει τα άτομα με HIV.
Η κλαριθρομυκίνη είναι διαθέσιμη με διάφορες εμπορικές ονομασίες ανά τον κόσμο, για παράδειγμα Truclar, Crixan, Claritt, Clarac, Biaxin, Klaricid, Klacid, Klaram, Klabax, Claripen, Clarem, Claridar, Fromilid, Clacid, Clacee, Vikrol, Infex, Clariwin, Resclar, Ranbaxy, Clarihexal και Clarinova.
Στην κλινική δοκιμή CLARICOR, οι ερευνητές ανακάλυψαν αύξηση της θνησιμότητας μεταξύ ασθενών με στεφανιαία νόσο, οι οποίοι υποβλήθηκαν σε θεραπεία με κλαριθρομυκίνη χρονικής διάρκειας δύο εβδομάδων.
Δεν είναι σαφές γιατί το αντιβιοτικό μπορεί να έχει ως αποτέλεσμα αυξημένο κίνδυνο θανάτου σε σύγκριση με το εικονικό φάρμακο, σύμφωνα με την ανακοίνωση του FDA.
Ορισμένες μελέτες παρατήρησης έχουν δείξει ότι η κλαριθρομυκίνη συνδέεται με αύξηση της θνησιμότητας και καρδιαγγειακών εκδηλώσεων, ενώ άλλες όχι. Ωστόσο, όλες οι μελέτες είχαν περιορισμούς σχεδιασμού, σύμφωνα με τον FDA. Από τις 6 μελέτες παρατήρησης, 2 βρήκαν ενδείξεις μακροχρόνιων κινδύνων από τη λήψη κλαριθρομυκίνης μεταξύ των ασθενών με ή χωρίς καρδιακή νόσο, ενώ οι 4 δεν βρήκαν.
Συνολικά, ο FDA έκρινε ότι τα αποτελέσματα της δοκιμής CLARICOR παρείχαν ισχυρές ενδείξεις πως η κλαριθρομυκίνη μπορεί να αυξήσει τους κινδύνους σε σύγκριση με άλλες μελέτες παρατήρησης.
Ως αποτέλεσμα αυτών των ευρημάτων, ο FDA πρόσθεσε μια προειδοποίηση σχετικά με τον αυξημένο κίνδυνο θνησιμότητας σε ασθενείς με στεφανιαία νόσο.Αυτά τα αποτελέσματα προστέθηκαν στις οδηγίες χρήσης του φαρμάκου που αναφέροιυν τις παρενέργειες της κλαριθρομυκίνης, σύμφωνα με την ανακοίνωση.
Στο πλαίσιο της συνεχούς παρακολούθησης, ο FDA σχεδιάζει να συνεχίσει την παρακολούθηση των εκθέσεων ασφαλείας για τους ασθενείς που λαμβάνουν κλαριθρομυκίνη.
Ο οργανισμός συμβουλεύει τους γιατρούς να ζυγίζουν τα οφέλη και τις παρενέργειες του φαρμάκου σε όλους τους ασθενείς και ειδικά σε εκείνους με στεφανιαία νόσο, ακόμη και όταν πρόκειται για μικρό χρονικό διάστημα, εξετάζοντας άλλα διαθέσιμα αντιβιοτικά για τη θεραπεία.
Επίσης, οι γιατροί θα πρέπει να ενημερώνουν τους ασθενείς με καρδιακή νόσο για τα σημεία και συμπτώματα των καρδιαγγειακών προβλημάτων, ανεξάρτητα από το λόγο χρήσης της κλαριθρομυκίνης.
Οι αξιωματούχοι της FDA παροτρύνουν τους ασθενείς και τους γιατρούς να ενημερώνουν για τυχόν παρενέργειες του φαρμάκου. Οι ασθενείς πάντως δεν πρέπει να διακόπτουν τη θεραπεία με αντιβιοτικά χωρίς να συμβουλεύονται τον παροχέα υπηρεσιών υγείας τους γιατί αυτό μπορεί να αποβεί εις βάρος της υγείας τους.
Πηγή: Clarithromycin (Biaxin): Drug Safety Communication – Potential Increased Risk of Heart Problems or Death in Patients With Heart Disease [FDA safety communication]. FDA website. February 22, 2018.